Un hombre de 32 años con infección por el virus de la inmunodeficiencia humana (VIH) fue ingresado en un hospital en Durban, Sudáfrica, debido a disnea y tos.
Cinco meses antes del ingreso, el paciente fue atendido en una clínica ambulatoria en Sudáfrica para la evaluación de una lesión en el párpado superior izquierdo. En el examen, se observaron lesiones elevadas y violáceas en el párpado izquierdo y en el lado derecho del tórax (Figura 1A).
Figura 1
Aspecto físico y examen patológico de la lesión torácica.
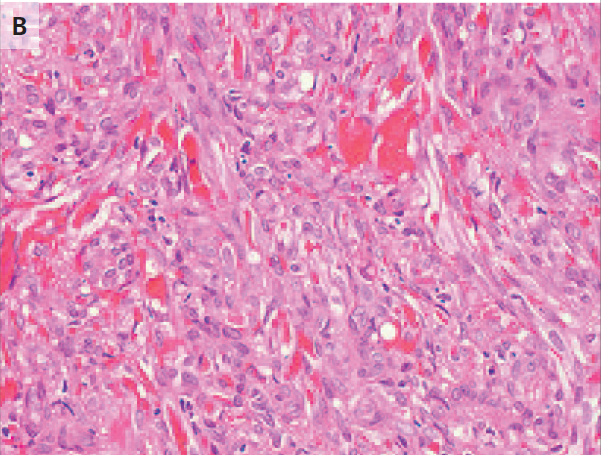
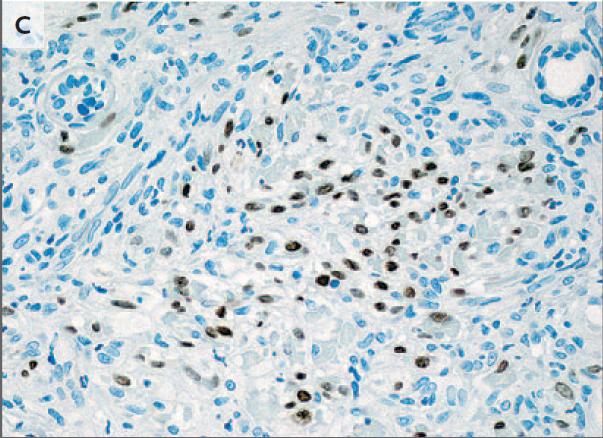
Una fotografía de la piel del paciente muestra lesiones elevadas y violáceas que son representativas de la lesión extirpada del lado derecho del tórax (Panel A). El examen patológico de una muestra de la piel del paciente muestra un tumor vasoformativo maligno que se compone de un infiltrado nodular de células fusiformes dispuesto en haces cortos entrelazados, con vasculatura interviniente y focos angiomatosos (Panel B, hematoxilina y eosina), características sugerentes de Sarcoma de Kaposi. La tinción inmunohistoquímica para el herpesvirus humano 8 muestra una inmunorreactividad nuclear en las células fusiformes y confirma el diagnóstico de sarcoma de Kaposi (Panel C).
El examen patológico de una muestra de biopsia por escisión de la lesión torácica mostró un tumor vasoformativo maligno de la dermis. El tumor estaba compuesto por un infiltrado nodular de células fusiformes dispuesto en haces cortos, entrelazados, con vasculatura intermedia y focos angiomatosos. El pigmento de hemosiderina intratumoral, la extravasación de eritrocitos, los glóbulos hialinos y el infiltrado linfoplasmocítico fueron hallazgos notorios (Figura 1B). La tinción inmunohistoquímica para el herpesvirus humano 8 (HHV-8) confirmó la inmunorreactividad nuclear en las células fusiformes (Figura 1C). Estos hallazgos fueron consistentes con un diagnóstico de sarcoma de Kaposi.
Una prueba de anticuerpos fue positiva para VIH tipo 1 (VIH-1) y el recuento de linfocitos T CD4 fue de 330 por milímetro cúbico (rango de referencia, 500 a 2010). En preparación para el inicio de la terapia antirretroviral (ART), el paciente completó las clases de pretratamiento. Durante los siguientes 3 meses, nuevas lesiones en la piel aparecieron en los muslos.
Dieciséis semanas antes del ingreso se instaló una tos productiva. Dos semanas más tarde, una muestra de esputo fue negativa para Mycobacterium tuberculosis mediante pruebas de reacción en cadena de polimerasa (PCR) y tinción y cultivo de bacilos ácido-alcohol resistentes. El recuento de linfocitos T CD4 fue de 268 por milímetro cúbico.
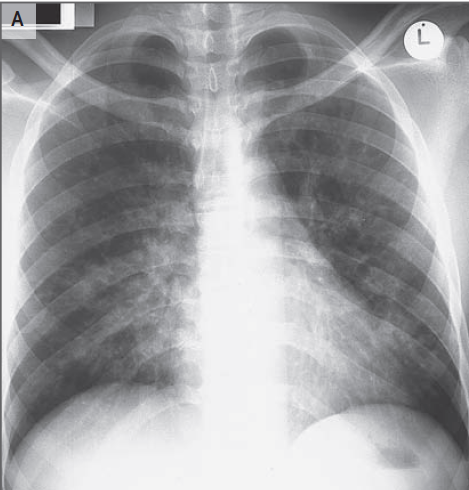
Una radiografía de tórax obtenida 14 semanas antes del ingreso mostró opacidades nodulares, de 5 a 7 mm de diámetro, en ambos pulmones, más prominentes en las zonas media e inferior; había pérdida de definición del hilio derecho, con engrosamiento peribroncovascular irregular y broncogramas aéreos. No se observaron derrames pleurales, linfadenopatías hiliares ni masas paraespinales (Figura 2A).
Figura 2
Radiografías de tórax.
Una radiografía de tórax obtenida 14 semanas antes del ingreso (Panel A) muestra opacidades micronodulares reticulares y mal definidas bilaterales en las zonas media e inferior, con predominio peribroncovascular y perihilar. Hay densidades ddifuminadas peribronquiales bilaterales. La opacificación parcial y los broncogramas aéreos son evidentes en la zona inferior derecha y el borde derecho del corazón está oculto, lo que indica una patología en el lóbulo medio derecho. En el segmento lingular del lóbulo superior izquierdo, hay una opacificación pobremente marginada, y el borde izquierdo del corazón está parcialmente oculto. No se pueden observar linfadenopatías mediastínicas ni derrames pleurales. Una radiografía de tórax obtenida en el ingreso (Panel B) muestra una progresión marcada de los hallazgos anteriores, con una consolidación coalescente perihiliar central y peribronchovascular extensa y bordes irregulares. Hay un marcado aumento en el tamaño y la profusión de las opacidades reticulonodulares.
Once semanas antes del ingreso, se inició el tratamiento con tenofovir, lamivudina y efavirenz. Una radiografía de tórax en el momento del inicio de la TAR no reveló cambios. Una semana después, el paciente fue atendido en la clínica de enfermedades infecciosas del hospital para evaluar el empeoramiento de la tos productiva, fiebres diarias de 2 semanas de duración, pérdida de peso de 2 kg y sudores nocturnos. Informó de una adherencia total al régimen de ART y no observó ningún cambio en las lesiones de la piel durante la semana en que recibió terapia.
En el examen, la temperatura era normal. Se observaron pequeñas lesiones violáceas en el párpado superior izquierdo y los muslos, con una cicatriz quirúrgica curada en el lado derecho del tórax. Los pulmones y el resto del examen fueron normales. Se obtuvieron muestras adicionales de esputo; Las pruebas de PCR y la tinción de bacilos ácido-alcohol resistentes y los cultivos para M. tuberculosis fueron negativos. El paciente volvió a su casa. Los síntomas persistieron y se realizó un diagnóstico presuntivo de tuberculosis pulmonar. Siete semanas antes del ingreso, se inició la administración de rifampicina, pirazinamida, etambutol e isoniazida.
El empeoramiento de la disnea, la tos, el malestar, la anorexia y una pérdida de peso adicional de 8 kg se desarrollaron durante las siguientes 7 semanas y el paciente ingresó en el hospital. Informó un aumento en el número de lesiones en la piel desde su última visita, 10 semanas antes. Había tenido una masa indolora en la región inguinal izquierda durante los últimos 5 años, que creía que era una hernia causada por el levantamiento de pesas. Aproximadamente 3 semanas después del inicio del tratamiento antirretroviral, la masa "hizo erupción" y drenó material purulento. Los medicamentos al ingreso incluían medicamentos antirretrovirales y antituberculosos. El paciente había nacido y vivía en Sudáfrica. Informó ser heterosexual y monógamo con su esposa. Había bebido alcohol socialmente hasta el inicio de esta enfermedad; No fumaba ni usaba drogas ilícitas. Según informes, sus padres murieron de vejez; Sus cinco hermanos estaban sanos. No tenía ninguna exposición conocida a la tuberculosis.
En el examen, el paciente impresionaba caquéctico, con pérdida de grasa temporal. La saturación de oxígeno osciló entre el 93% y el 96% mientras respiraba aire ambiente, y aparecía disnea con mínimos esfuerzos. La presión arterial fue de 95/63 mm Hg y el pulso de 120 latidos por minuto. Había crepitaciones sobre los campos pulmonares izquierdo medio e inferior; el borde del hígado era palpable 2 cm por debajo del margen costal, y la punta del bazo era palpable. Se encontraron lesiones cutáneas viscosas en las piernas, brazos, torso, paladar y párpado izquierdo. Había linfadenopatía en las regiones cervical y axilar, con un ganglio linfático que drenaba actualmente y un signo del surco (separación visible de ganglios linfáticos inguinales y femorales agrandados por el ligamento inguinal) en la ingle izquierda.
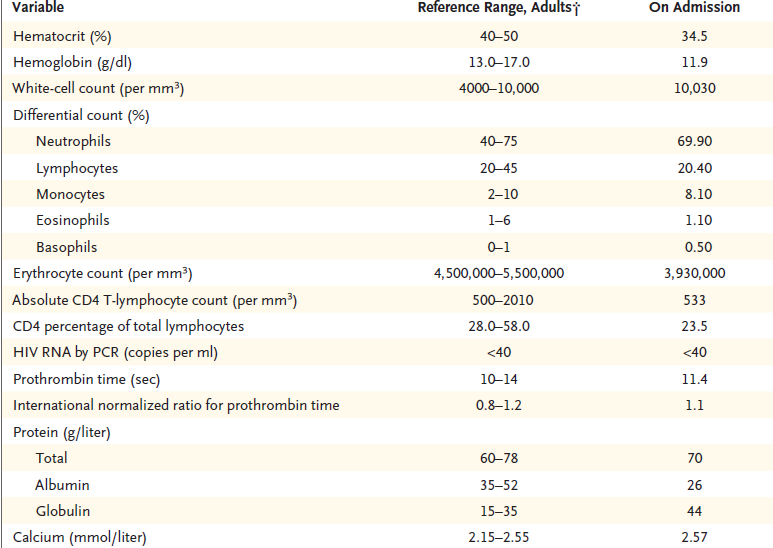
Los niveles en sangre de electrolitos, bilirrubina, fósforo, magnesio, fosfatasa alcalina y alanina aminotransferasa fueron normales, al igual que el recuento de plaquetas, los índices de glóbulos rojos y los resultados de las pruebas de función renal. Los resultados de las pruebas de detección de los virus de la hepatitis A y B fueron compatibles con la inmunidad frente a la exposición previa de estos agentes, y los resultados de la detección del virus de la hepatitis C fueron negativos; Otros resultados se muestran en la Tabla 1.
TABLA 1
Datos de laboratorio.
Una radiografía de tórax mostró una progresión marcada de los hallazgos radiológicos anteriores (Figura 2B). Había una extensa consolidación perihiliar central y confluente peribroncovascular. Se observaron opacidades nodulares irregulares en la periferia de ambos campos pulmonares, y algunas en el lóbulo superior izquierdo mostraron una posible cavitación o broncogramas aéreos. No había derrames pleurales.
Dada esta constelación de hallazgos radiológicos en un paciente inmunocomprometido con sarcoma de Kaposi cutáneo, el diagnóstico diferencial incluye linfoma, sarcoma de Kaposi y síndrome inflamatorio de reconstitución inmune asociado a sarcoma de Kaposi (IRIS). La tuberculosis atípica y las infecciones por Pneumocystis jirovecii podrían ser otras consideraciones.1-3
La tinción de Gram de una muestra de esputo reveló escasos cocos grampositivos, y en un cultivo se desarrolló una flora respiratoria normal; La tinción de Ziehl-Neelsen y auramina, las pruebas de anticuerpos de fluorescencia directa para P. jirovecii y un cultivo de micobacterias fueron negativos. Se continuó con la administración de medicamentos antirretrovirales y antituberculosos, y se agregaron doxiciclina, trimetoprim-sulfametoxazol, prednisona y oxígeno (40%, administrados a través de una mascarilla facial sin réplica).
Se realizaron procedimientos diagnósticos.
DIAGNÓSTICO DIFERENCIAL
Aunque el diagnóstico diferencial de la enfermedad pulmonar progresiva en una persona con infección por VIH-1 es amplio, varias pistas en este caso me permitirán concentrarme en relativamente pocas entidades. El recuento de linfocitos T CD4 del paciente en la presentación, el ritmo de progresión de la enfermedad, los sistemas de órganos involucrados y la geografía deben considerarse al formular un diagnóstico diferencial.
Este paciente presentó un sarcoma de Kaposi localizado y un recuento inicial de células T CD4 de 330 por milímetro cúbico. Un recuento posterior de células T CD4 fue de 268 por milímetro cúbico, antes del inicio del tratamiento antirretroviral. A pesar de un fuerte aumento en el recuento a 533 células por milímetro cúbico después del inicio de la terapia, la enfermedad progresó clínica y radiográficamente. Debido a que el recuento de células T CD4 fue más alto que los que suelen estar asociados con las infecciones oportunistas comunes que se observan en personas con el síndrome de inmunodeficiencia adquirida (SIDA), centraré mi diagnóstico diferencial en entidades que ocurren en personas con recuentos celulares de céluas T CD4 más alto. El sarcoma de Kaposi y otros cánceres, así como ciertas infecciones bacterianas, especialmente la tuberculosis, son las enfermedades que ocurren con mayor frecuencia en esta etapa de la infección. Me parece útil pensar que el momento en que aparecen las complicaciones de la enfermedad del VIH está inversamente relacionado con la virulencia del agente infeccioso. Las complicaciones más tempranas suelen ocurrir con organismos más virulentos y continúan aumentando cada vez más a lo largo del curso restante de la historia natural de la enfermedad del VIH, mientras que los agentes menos virulentos comienzan a aparecer a medida que el sistema inmunitario se debilita cada vez más. Dado el declive progresivo de este paciente con un recuento de células T CD4 relativamente alto, consideraré las enfermedades que ocurren temprano con una presentación agresiva.
La progresión de la enfermedad de este paciente, desde subaguda a crónica, también puede proporcionar una pista diagnóstica. La enfermedad parece haber progresado durante un período de 5 meses, desde el descubrimiento de las lesiones de la piel del sarcoma de Kaposi hasta una aceleración más rápida de la enfermedad sistémica grave. Este patrón es consistente con el sarcoma de Kaposi progresivo, aunque otros cánceres, la tuberculosis y otras enfermedades infecciosas lentamente progresivas siguen siendo posibles.
La presentación de esta paciente se caracteriza por enfermedad cutánea y pulmonar. Si bien pudo haber tenido múltiples dos afecciones concurrentes, si intentamos explicar su presentación con un proceso único y unificador, debemos centrar nuestro diagnóstico diferencial en entidades que causan enfermedades sistémicas con afectación tanto de la piel como de los pulmones.
Por último, el contexto geográfico de la enfermedad del paciente es de gran valor diagnóstico. Este paciente es de Sudáfrica, un país que sufre la epidemia de VIH / SIDA más grave del mundo y las epidemias de tuberculosis concurrentes. Deberíamos intentar ajustar la enfermedad clínica de este paciente en el contexto de las entidades de enfermedad que se observan con mayor frecuencia en Sudáfrica.
¿Qué diagnósticos específicos tendrían estas características? El ya conocido en este paciente es el sarcoma de Kaposi, inicialmente diagnosticado por la aparición de algunas lesiones cutáneas características, elevadas y confirmadas en la biopsia. ¿Qué otros diagnósticos debemos tener en cuenta?
LINFOMA RELACIONADO CON EL SIDA
En este caso, se deben considerar los linfomas relacionados con el SIDA, incluidos el linfoma de células B grandes y el linfoma de Burkitt. Los síntomas y signos dependen del sitio de participación y de la etapa de la enfermedad, que puede ser variable. Al igual que con el sarcoma de Kaposi, los linfomas de células B se producen con mayor frecuencia en personas con infección por VIH y pueden ocurrir en personas con recuentos de células T CD4 más altos, y la progresión clínica de la enfermedad en la presentación suele ser subaguda. Síntomas B como fiebre, pérdida de peso y sudores nocturnos. La afectación de la piel es inusual y predomina la enfermedad visceral, particularmente en el tracto gastrointestinal y el sistema nervioso central. La enfermedad pulmonar, que tuvo este paciente, es menos frecuente. Las anomalías hematológicas mínimas y la ausencia de adenopatías viscerales prominentes también argumentan contra el linfoma. Estas características de la enfermedad del paciente hacen que el linfoma relacionado con el SIDA sea posible pero poco probable.
TUBERCULOSIS
La tuberculosis debe ser la más alta en nuestra lista de diagnósticos. La tuberculosis es la causa más común de enfermedades y muerte asociadas con el VIH en todo el mundo.5 En áreas del mundo y en poblaciones específicas con una alta prevalencia tanto de VIH como de M. tuberculosis, suelen aparecer epidemias de tuberculosis. En Sudáfrica, la incidencia de la tuberculosis se acerca a 1000 personas por cada 100,000 habitantes, 5 en contraste con 3 a 4 por 100,000 habitantes en los Estados Unidos. En la provincia de KwaZulu-Natal, donde residía este paciente, las tasas superan las 1000 personas por 100,000. En la población rural de los zulúes, la presencia de tuberculosis a menudo conduce al diagnóstico de infección por el VIH, y comúnmente se dice que "la tuberculosis es la madre del SIDA".
Este paciente tiene muchas características de la tuberculosis. El riesgo de tuberculosis activa comienza con un mayor recuento de células T CD4 y aumenta progresivamente a medida que disminuye el recuento de células T CD4. El ritmo de la progresión de la enfermedad es subagudo, y son característicos la tos crónica, la fiebre, los sudores nocturnos y la pérdida de peso. Aunque la tuberculosis está en nuestra lista de diagnósticos, la presencia de disnea grave en el esfuerzo, los hallazgos radiológicos atípicos y los resultados negativos de las pruebas micobacteriológicas reducen la probabilidad. El frotis de esputo a menudo es falsamente negativo en pacientes coinfectados con tuberculosis y VIH, como resultado de la enfermedad paucibacilar en los pulmones y las secreciones pulmonares. Las pruebas de PCR son más sensibles, con tasas de positividad tan altas como 75% en pacientes coinfectados.6 En este caso, las pruebas de PCR se realizaron y fueron negativas. El cultivo para M. tuberculosis sigue siendo el estándar y fue negativo en dos ocasiones. La tuberculosis extrapulmonar también es común en pacientes con tuberculosis y coinfección por VIH. Las pruebas de diagnóstico realizadas en este caso no pudieron descartar la tuberculosis extrapulmonar, pero la afectación predominante del paciente del sistema de órganos viscerales fue pulmonar, y creo que los resultados del examen de esputo fueron adecuados para hacer que este diagnóstico sea poco probable.
El paciente recibió tratamiento antituberculoso empírico sin mejoría durante un período de 2 meses, lo que reduce la probabilidad de que tuviera tuberculosis, a menos que tuviera tuberculosis farmacorresistente. No tenía antecedentes de exposición previa a medicamentos antituberculosos; por lo tanto, el origen de la tuberculosis farmacorresistente se habría producido a través de la transmisión reciente de otra persona al cuidado de la salud o en un entorno comunitario, 7,8, que es un hecho bien documentado y frecuente en Sudáfrica. Sin embargo, sus cultivos de esputo negativos hacen esto poco probable.
SARCOMA DE KAPOSI
El sarcoma de Kaposi parece encajar bien en el marco contextual del recuento de células T CD4, el ritmo de la progresión de la enfermedad, la localización de la afectación del sistema de órganos y la geografía. Cuando este paciente se presentó, su recuento de células T CD4 estaba muy por encima de 200 por milímetro cúbico. La enfermedad cambió de localizada e indolente a subaguda, con algunas lesiones cutáneas características que aumentaron rápidamente en número, con afectación de la mucosa; progresó a fiebre, pérdida de peso, sudores nocturnos y afectación pulmonar extensa, con disnea severa en el esfuerzo. Todo esto ocurrió en el África subsahariana en el contexto de una incidencia creciente del sarcoma de Kaposi asociado con la epidemia de la enfermedad del VIH.
En entornos con privilegios de recursos, la incidencia del sarcoma de Kaposi ha disminuido drásticamente con la disponibilidad de TAR. En contraste, en África subsahariana, donde la epidemia de VIH-SIDA y la inmunosupresión asociada están aumentando y la disponibilidad de TAR es limitada, la incidencia del sarcoma de Kaposi se ha acelerado dramáticamente. Esto es particularmente cierto en las regiones geográficas que tienen una prevalencia de HHV-8, el agente causal del sarcoma de Kaposi y VIH-1.9,10. Entre las personas con infección por VIH, el riesgo de sarcoma de Kaposi es 10.000 veces mayor que el riesgo entre personas sin infección por VIH11; El sarcoma de Kaposi se ha convertido en uno de los cánceres más comunes en el África subsahariana. Las manifestaciones pulmonares del sarcoma de Kaposi están bien descritas e incluyen infiltrados progresivos y disnea, como se observa en este paciente12,13.
¿Podría explicarse el curso clínico de este paciente por la presencia tanto del sarcoma de Kaposi como de la tuberculosis, dadas las altas tasas de ambas enfermedades, su superposición geográfica y las características clínicas que se mencionan? Esto es ciertamente posible. La coexistencia del sarcoma de Kaposi y la tuberculosis es común en pacientes con VIH en el África subsahariana. En un estudio descriptivo realizado en un importante hospital de referencia en Durban, se demostró que un tercio de los 152 pacientes consecutivos en los que se diagnosticó el sarcoma de Kaposi tenía una infección oportunista adicional, con mayor frecuencia tuberculosis14.
SÍNDROME INFLAMATORIO DE RECONSTITUCIÓN INMUNE ASOCIADA AL SARCOMA DE KAPOSI
Una de las características más destacadas del curso clínico del paciente fue el deterioro de su condición después del inicio de un TAR altamente activo. El tratamiento antirretroviral solo puede mejorar e incluso revertir las lesiones del sarcoma de Kaposi, pero no de manera invariable y, a menudo, muy lentamente.14,15 Un evento adicional probable que podría explicar el empeoramiento del paciente es el IRIS asociado a sarcoma de Kaposi. 16,17 Esta entidad no es infrecuente y puede ser grave o incluso fatal.14
No existe una prueba de laboratorio para confirmar el diagnóstico y, en este caso, se deben descartar otras entidades, como se hizo para la tuberculosis. Sin embargo, tanto la sincronización del deterioro del estado del paciente después del inicio de la terapia antirretroviral como la expansión clínica de las lesiones existentes del sarcoma de Kaposi son más consistentes con el diagnóstico de IRIS asociado al sarcoma de Kaposi. El tratamiento con agentes antiinflamatorios, particularmente glucocorticoides, puede mejorar el proceso de la enfermedad. El procedimiento de diagnóstico que confirmaría el diagnóstico es una broncoscopia, con inspección de lesiones bronquiales y consideración de biopsia transbronquial si no se observan lesiones.
Cuando a este hombre de 32 años con infección por VIH, fue evaluado preocupaba la evolución bastante rápida de sus síntomas pulmonares. Sobre la base de su diagnóstico conocido de sarcoma de Kaposi cutáneo, se pensó que la afectación pulmonar por el sarcoma de Kaposi era la explicación más probable para la rápida progresión de la enfermedad. Sin embargo, dado que la neumonía por P. jirovecii y la tuberculosis son tan comunes, no podríamos descartar estos diagnósticos sin pruebas más definitivas. Además, la relación temporal entre su deterioro clínico y el inicio del tratamiento antirretroviral hizo de IRIS una posibilidad probable. IRIS se considera una manifestación de desregulación inmune.18 La respuesta inflamatoria específica del HHV-8 inducida por ART puede dar lugar a un aumento de las citocinas y quimiocinas proinflamatorias que regulan la expresión de los factores angioproliferativos y tumorigénicos.19 Esto a su vez puede resultar en una paradoja empeoramiento del VIH preexistente: sarcoma de Kaposi (IRIS asociado al sarcoma de Kaposi paradójico). Los criterios para el diagnóstico de IRIS asociado a sarcoma de Kaposi pulmonar incluyen sarcoma de Kaposi probado en biopsia en un sitio extrapulmonar con una radiografía de tórax que empeora de otra manera inexplicable, lesiones mucocutáneas consistentes con el sarcoma de Kaposi que ocurren en asociación temporal con ART exitosa, o ambos. Este paciente tenía un sarcoma de Kaposi de piel comprobado por biopsia y un empeoramiento dramático de los hallazgos en la radiografía de tórax. Elegimos realizar una broncoscopia para un diagnóstico más definitivo del IRIS asociado a sarcoma de Kaposi.
DIAGNOSTICO CLINICO PRESUNTIVO
SARCOMA DE KAPOSI CUTÁNEO Y VISCERAL (PULMONAR).
SÍNDROME INFLAMATORIO DE RECONSTITUCIÓN INMUNE ASOCIADA AL SARCOMA DE KAPOSI.
DISCUSION PATOLOGICA
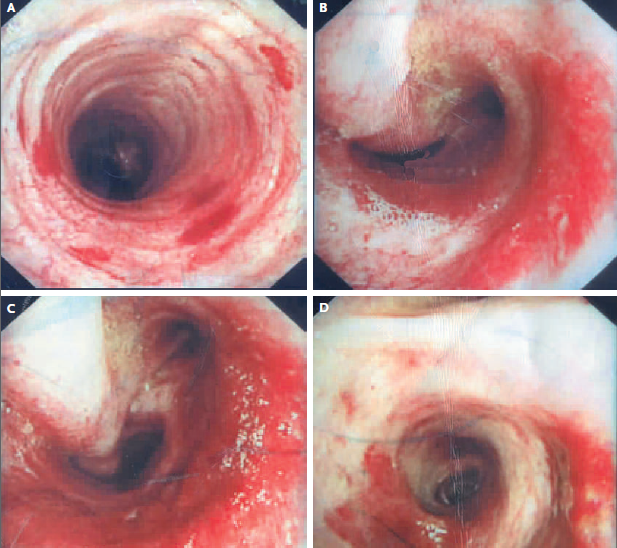
La inspección broncoscópica se considera el método más sensible para el diagnóstico del sarcoma de Kaposi pulmonar debido a la tendencia de esta afección a pasar de la capa subepitelial a la invasión de las superficies mucosas. Se realizó broncoscopia y nuestro primer hallazgo fue múltiples lesiones maculares rojas paralelas a los anillos traqueales (Figura 3A).
Figura 3
Evaluación broncoscópica de las vías aéreas.
Poco después del ingreso se realizó una evaluación broncoscópica de las vías respiratorias. Las imágenes del procedimiento muestran lesiones rojas maculares paralelas a los anillos traqueales (Panel A). Las lesiones se concentran en la carina traqueal (paneles B y C) y en el bronquio principal izquierdo (panel D). La aparición de estas lesiones es compatible con un diagnóstico de sarcoma de Kaposi.
También se observaron múltiples lesiones maculopapulares que se concentraron en la carina traqueal (Figura 3B y 3C) y el bronquio principal izquierdo (Figura 3D). La carina se extendió, sugiriendo una linfadenopatía subcarinal. Las lesiones endobronquiales del sarcoma de Kaposi son característicamente maculopapulares, de color púrpura rojizo, concentradas en las bifurcaciones de las vías respiratorias y paralelas a los anillos traqueales. En conjunto, estas características aumentaron nuestra sospecha clínica de sarcoma de Kaposi pulmonar.
No realizamos una biopsia porque generalmente no está indicada en las lesiones típicas del sarcoma de Kaposi. Una biopsia conlleva un riesgo del 30% de hemorragia clínicamente significativa, y el rendimiento diagnóstico de las biopsias broncoscópicas varía entre el 26 y el 60%, debido a la afectación de la submucosa parcheada.20 Sobre la base del aspecto broncoscópico característico de las lesiones, en combinación con Diagnóstico del sarcoma de Kaposi cutáneo, nuestro diagnóstico clínico fue el sarcoma de Kaposi pulmonar, probablemente complicado por IRIS.
MANEJO
Los pilares del tratamiento del sarcoma de Kaposi generalizado en un paciente con infección por VIH, como este, son el tratamiento antirretroviral y la quimioterapia. Todos los pacientes infectados con VIH que tienen sarcoma de Kaposi deben recibir TAR. Después del inicio de la terapia antirretroviral, los niveles plasmáticos de HHV-8 disminuyen debido a un aumento en las respuestas inmunitarias específicas de HHV-8. 16,21,22 El efecto de la terapia antirretroviral en HHV-8 y, por lo tanto, en la tumorigénesis, es muy probable que explique la dramática caída en la incidencia del sarcoma de Kaposi en los Estados Unidos desde que se introdujo el tratamiento antirretroviral efectivo allí. 23 Sin embargo, aunque el tratamiento antirretroviral por sí solo puede conducir a la regresión del sarcoma de Kaposi, en ocasiones las lesiones pueden empeorar, como se observa en este caso. Además, el sarcoma de Kaposi pulmonar continúa asociado con una alta tasa de mortalidad, incluso en la era de la TARV efectiva24.
Debido a que el sarcoma de Kaposi en este paciente empeoró mientras recibía tratamiento antirretroviral, era evidente que se necesitaba una terapia adicional. Las opciones quimioterapéuticas incluyen doxorubicina pegilada, daunorubicina liposomal o paclitaxel.25 Dado que estos medicamentos a menudo no están disponibles en entornos con recursos limitados, a veces se usan agentes alternativos, como una combinación de doxorubicina, bleomicina y vincristina (como en este caso) o etopósido oral.26 Aunque la terapia anti-HHV-8 con ganciclovir parece proteger a los pacientes con SIDA del desarrollo del sarcoma de Kaposi, 27,28 no existe un papel aparente para tal tratamiento una vez que se produce el sarcoma de Kaposi, 29 tal vez porque el HHV-8 es principalmente en forma latente en el momento en que se establece el tumor.
Una combinación de tratamiento antirretroviral y quimioterapia tiene un papel importante en algunos pacientes con sarcoma de Kaposi asociado con el VIH. La tasa general de supervivencia entre los pacientes con sarcoma de Kaposi que reciben TAR solo es similar a la tasa entre aquellos que reciben TARV más quimioterapia. Sin embargo, la terapia de combinación tiene una tasa de respuesta más alta y una tasa de supervivencia libre de progresión que el TAR solo14. Además, la tasa de muerte entre los pacientes con IRIS asociado a sarcoma de Kaposi es particularmente alta. Debido a la enfermedad generalizada, la afectación visceral sintomática y la evidencia de IRIS en este paciente, una combinación de TAR y quimioterapia sería apropiada.
Luego de los hallazgos negativos en el examen microbiológico del líquido de lavado broncoalveolar, se suspendió el tratamiento para neumocistis y tuberculosis. El paciente comenzó a recibir quimioterapia con doxorubicina, bleomicina y vincristina. Tuvo una mejoría dramática en los primeros 3 días de quimioterapia. Posteriormente fue remitido a otro hospital para recibir atención oncológica en curso. El paciente continuó recibiendo TAR y mantuvo una carga viral indetectable. Las lesiones de la piel comenzaron a mejorar poco después del inicio de la quimioterapia, con una resolución completa en el sexto ciclo (aproximadamente 16 semanas después del inicio).
Otra radiografía de tórax obtenida 25 semanas después de comenzar la quimioterapia mostró un retorno a la línea de base (Figura 4).
Figura 4
Radiografía de tórax, 25 semanas después de la admisión.
Hay una mejora notable, con una resolución casi completa de la opacificación perihiliar y peribronchovascular. Las opacidades reticulares bilaterales en las zonas pulmonares superior y media representan áreas de fibrosis.
Sin embargo, 7 semanas después de completar el sexto ciclo de quimioterapia (22 semanas después de comenzar la quimioterapia), aparecieron nuevas lesiones cutáneas en el lado derecho del tórax anterior y en el pie derecho, con hinchazón del párpado izquierdo. El paciente no tuvo ningún síntoma respiratorio y la radiografía de tórax se mantuvo normal. Fue referido para quimioterapia adicional.
Dentro de un mes después de la reanudación de la quimioterapia, todas las lesiones retrocedieron. Hasta la fecha, el paciente ha recibido un total de nueve ciclos de quimioterapia y permanece bien, sin lesiones cutáneas. Su última visita ambulatoria fue aproximadamente 9 meses después de la presentación.
DIAGNÓSTICO ANATÓMICO
SARCOMA DE KAPOSI COMPLICADO POR EL SÍNDROME INFLAMATORIO DE RECONSTITUCIÓN INMUNE.
Traducción de :
A 32-Year-Old HIV-Positive African Man with Dyspnea and Skin Lesions
Gerald H. Friedland, M.D., Pumersha Naidoo, M.B., B.Ch., Bilal Abdool-Gafoor, M.D., Mahomed-Yunus S. Moosa, M.D., Pratistadevi K. Ramdial, M.B., Ch.B., and Rajesh T. Gandhi, M.D.
N Engl J Med 2013; 369:1152-1161September 19, 2013DOI: 10.1056/NEJMcpc1305985
REFERENCES
1Godoy MC, Rouse H, Brown JA, Phillips P, Forrest DM, Muller NL. Imaging features of pulmonary Kaposi sarcoma-associated immune reconstitution syndrome. AJR Am J Roentgenol 2007;189:956-965
CrossRef | Web of Science | Medline
2Shah RM, Kaji AV, Ostrum BJ, Friedman AC. Interpretation of chest radiographs in AIDS patients: usefulness of CD4 lymphocyte counts. Radiographics 1997;17:47-58[Erratum, Radiographics 1997;17:804.]
Web of Science | Medline
3Sider L, Weiss AJ, Smith MD, VonRoenn JH, Glassroth J. Varied appearance of AIDS-related lymphoma in the chest. Radiology 1989;171:629-632
Web of Science | Medline
4Levine AM, Seneviratne L, Espina BM, et al. Evolving characteristics of AIDS-related lymphoma. Blood 2000;96:4084-4090
Web of Science | Medline
5Global tuberculosis report 2012. Geneva: World Health Organization, 2012.
6Boehme CC, Nicol MP, Nabeta P, et al. Feasibility, diagnostic accuracy, and effectiveness of decentralised use of the Xpert MTB/RIF test for diagnosis of tuberculosis and multidrug resistance: a multicentre implementation study. Lancet 2011;377:1495-1505
CrossRef | Web of Science | Medline
7Gandhi NR, Moll A, Sturm AW, et al. Extensively drug-resistant tuberculosis as a cause of death in patients co-infected with tuberculosis and HIV in a rural area of South Africa. Lancet 2006;368:1575-1580
CrossRef | Web of Science | Medline
8Shenoi SV, Escombe AR, Friedland G. Transmission of drug-susceptible and drug-resistant tuberculosis and the critical importance of airborne infection control in the era of HIV infection and highly active antiretroviral therapy rollouts. Clin Infect Dis 2010;50:Suppl 3:S231-S237
CrossRef | Web of Science | Medline
9Mosam A, Hurkchand HP, Cassol E, et al. Characteristics of HIV-1-associated Kaposi's sarcoma among women and men in South Africa. Int J STD AIDS 2008;19:400-405
CrossRef | Web of Science | Medline
10Mosam A, Carrara H, Shaik F, et al. Increasing incidence of Kaposi's sarcoma in black South Africans in KwaZulu-Natal, South Africa (1983-2006). Int J STD AIDS 2009;20:553-556
CrossRef | Web of Science | Medline
11Dezube BJ. Clinical presentation and natural history of AIDS-related Kaposi's sarcoma. Hematol Oncol Clin North Am 1996;10:1023-1029
CrossRef | Web of Science | Medline
12Garay SM, Belenko M, Fazzini E, Schinella R. Pulmonary manifestations of Kaposi's sarcoma. Chest 1987;91:39-43
CrossRef | Web of Science | Medline
13Aboulafia DM. The epidemiologic, pathologic, and clinical features of AIDS-associated pulmonary Kaposi's sarcoma. Chest 2000;117:1128-1145
CrossRef | Web of Science | Medline
14Mosam A, Shaik F, Uldrick TS, et al. A randomized controlled trial of highly active antiretroviral therapy versus highly active antiretroviral therapy and chemotherapy in therapy-naive patients with HIV-associated Kaposi sarcoma in South Africa. J Acquir Immune Defic Syndr 2012;60:150-157
CrossRef | Web of Science | Medline
15Bower M, Weir J, Francis N, et al. The effect of HAART in 254 consecutive patients with AIDS-related Kaposi's sarcoma. AIDS 2009;23:1701-1706
CrossRef | Web of Science | Medline
16Bihl F, Mosam A, Henry LN, et al. Kaposi's sarcoma-associated herpesvirus-specific immune reconstitution and antiviral effect of combined HAART/chemotherapy in HIV clade C-infected individuals with Kaposi's sarcoma. AIDS 2007;21:1245-1252
CrossRef | Web of Science | Medline
17Letang E, Almeida JM, Miro JM, et al. Predictors of immune reconstitution inflammatory syndrome-associated with Kaposi sarcoma in Mozambique: a prospective study. J Acquir Immune Defic Syndr 2010;53:589-597
Web of Science | Medline
18Foudraine NA, Hovenkamp E, Notermans DW, et al. Immunopathology as a result of highly active antiretroviral therapy in HIV-1-infected patients. AIDS 1999;13:177-184
CrossRef | Web of Science | Medline
19Lawn SD, Meintjes G. Pathogenesis and prevention of immune reconstitution disease during antiretroviral therapy. Expert Rev Anti Infect Ther 2011;9:415-430
CrossRef | Web of Science | Medline
20Yoo DJ, Lee KH, Munderi P, Shin KC, Lee JK. Clinical and bronchoscopic findings in Ugandans with pulmonary Kaposi's sarcoma. Korean J Intern Med 2005;20:290-294
CrossRef | Medline
21Sullivan SG, Hirsch HH, Franceschi S, et al. Kaposi sarcoma herpes virus antibody response and viremia following highly active antiretroviral therapy in the Swiss HIV Cohort study. AIDS 2010;24:2245-2252
CrossRef | Web of Science | Medline
22Borok M, Fiorillo S, Gudza I, et al. Evaluation of plasma human herpesvirus 8 DNA as a marker of clinical outcomes during antiretroviral therapy for AIDS-related Kaposi sarcoma in Zimbabwe. Clin Infect Dis 2010;51:342-349
CrossRef | Web of Science | Medline
23Engels EA, Pfeiffer RM, Goedert JJ, et al. Trends in cancer risk among people with AIDS in the United States 1980-2002. AIDS 2006;20:1645-1654
CrossRef | Web of Science | Medline
24Palmieri C, Dhillon T, Thirlwell C, et al. Pulmonary Kaposi sarcoma in the era of highly active antiretroviral therapy. HIV Med 2006;7:291-293
CrossRef | Web of Science | Medline
25Dittmer DP, Richards KL, Damania B. Treatment of Kaposi sarcoma-associated herpesvirus-associated cancers. Front Microbiol 2012;3:141-141
CrossRef
26Krown SE. Treatment strategies for Kaposi sarcoma in sub-Saharan Africa: challenges and opportunities. Curr Opin Oncol 2011;23:463-468
CrossRef | Web of Science | Medline
27Mocroft A, Youle M, Gazzard B, Morcinek J, Halai R, Phillips AN. Anti-herpesvirus treatment and risk of Kaposi's sarcoma in HIV infection. AIDS 1996;10:1101-1105
CrossRef | Web of Science | Medline
28Glesby MJ, Hoover DR, Weng S, et al. Use of antiherpes drugs and the risk of Kaposi's sarcoma: data from the Multicenter AIDS Cohort Study. J Infect Dis 1996;173:1477-1480
CrossRef | Web of Science | Medline
29Krown SE, Dittmer DP, Cesarman E. Pilot study of oral valganciclovir therapy in patients with classic Kaposi sarcoma. J Infect Dis 2011;203:1082-1086
CrossRef | Web of Science | Medline